Lange-QT-syndroom: verschil tussen versies
Geen bewerkingssamenvatting |
Geen bewerkingssamenvatting |
||
| Regel 225: | Regel 225: | ||
*Hypokaliëmie | *Hypokaliëmie | ||
*Bradycardie | *Bradycardie | ||
*Recente conversie van [[ | *Recente conversie van [[Boezemfibrilleren|boezemfibrilleren]], in het bijzonder als er een QT verlengend medicijn is gebruikt (sotalol, amiodarone) | ||
*Decompensatio cordis | *Decompensatio cordis | ||
*Digitalisbehandeling | *Digitalisbehandeling | ||
Huidige versie van 10 jul 2017 13:42
Het lange-QT-syndroom betreft een aandoening waarbij, zoals de naam al doet vermoeden, de QT-tijd op het ecg verlengd is. Dit kan aangeboren zijn, maar ook verworven. Bij een verlengde QT-tijd is de repolarisatie vertraagd. Dat wil zeggen dat de hartcellen langer nodig hebben om zich klaar te maken voor de volgende slag. Als er een nieuwe hartslag komt, terwijl nog niet alle hartcellen daar klaar voor zijn, kunnen ernstige ritmestoornissen ontstaan, zoals Torsade de Pointes en ventrikelfibrilleren.
Diagnose en behandeling
De diagnose wordt gesteld aan de hand van het ecg. Hierbij kijkt men naar het QT-interval als mede naar de T-golven (repolarisatie). Soms is de QT-tijd lastig te bepalen. Kijk hier voor het meten van de QT-tijd bij afwijkende QT-patronen. Een QTc van > 500 ms bij patiënten met het lange-QT-syndroom is geassocieerd met een verhoogd risico op cardiale events. Omdat de QTc kan wisselen over de jaren, is het belangrijk ecg's te herhalen over de tijd en de langst gemeten QTc te gebruiken bij risico-inschatting. [1]
Voor de behandeling zijn er een aantal mogelijkheden:[2]
- "Lifestyle modification":
- Geen sport in competitieverband bij alle patiënten met LQTS
- Niet zwemmen in geval van LQT1
- Nachtelijk lawaai voorkómen in geval van LQT2 (bijvoorbeeld van telefoon of wekker)
- medicatie: bètablokkers. Bètablokkers verminderen het optreden van plotselinge hartdood bij patiënten, waarbij een genetische afwijking is gevonden passend bij LQTS, maar bij wie geen verlengd QT-interval op het ecg is te zien.
- ICD-implantatie in combinatie met een bètablokker bij LQTS-patiënten met een eerdere hartstilstand of met syncope of ventrikeltachycardiën ondanks bètablokkers.
Aangeboren LQTS
Congenitale LQTS is een erfelijke aandoening waarbij de ventriculaire repolarisatie verlengd is, wat zich onder meer uit in een verlengde QT-tijd op het ecg. Syncope en plotse hartdood treedt bij LQTS vaak op tijdens een specifieke ventriculaire ritmestoornis: Torsade de Pointes. Hierbij draait de hartas continu, tijdens een ventriculaire tachycardie. Torsade de Pointes kan overgaan in ventrikelfibrilleren en plotse hartdood. De prevalentie is ongeveer 1:3000-5000. De symptomen starten vaak in de tienerleeftijd. Niet alle dragers van afwijkende LQTS-genen zijn ook ziek. De uiting kan wisselen van extreme QT-verlenging en regelmatige syncope, tot minimaal verlengde QT-tijd, zonder enig symptoom.
Onderzoek heeft aangetoond, dat de aangeboren vormen berusten op een genetisch defect in de genen die coderen voor ionenstromen die verantwoordelijk zijn voor de repolarisatiefase van een actiepotentiaal. He meest voorkomende defect berust op die van de uitwaartse kaliumstroom. Dit leidt tot een verlengde repolarisatie en dus een verlengde QT-tijd. Tevens bestaan er ook defecten in de natriumkanalen. Er is dan met name sprake van een langere inwaartse natriumstroom. Het gevolg is een langere actiepotentiaal alsmede een langere QT-tijd.
Er zijn inmiddels 8 LQTS-genen beschreven met ieder verschillende kenmerken:
| type | chromosoom | gen (met OMIM-links) | eiwit | ionkanaal | frequentie | SCD-incidentie | overerving | ecg-kenmerken | trigger | eponiem |
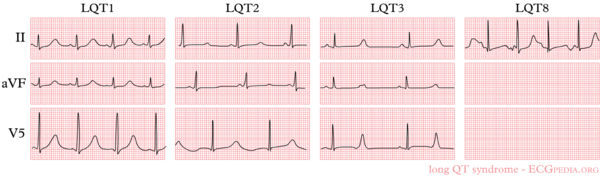
| LQTS1 | 11p15 | KCNQ1 | KvLQT1 | Iks | ~ 50% | 0,30%/jaar | AD, AR | 'early onset' T-top met brede basis | inspanning, m.n. zwemmen | JLN1 indien homozygoot, LQTS1 indien heterozygoot |
|---|---|---|---|---|---|---|---|---|---|---|
| LQTS2 | 7q35 | KCNH2 | hERG | Ikr | 30-40% | 0,60%/jaar | AD | kleine, late T-top | adrenerge prikkels, m.n. nachtelijk lawaai | JLN2 indien homozygoot, LQTS2 indien heterozygoot |
| LQTS3 | 3p21 | SCN5A | Na-kanaal | 5-10% | 0,56%/jaar | AD | 'late onset' T-golf van normale vorm | |||
| LQTS4 | 4q25 | ANK2 | Ankyrin B | < 1% | AD | |||||
| LQTS5 | 21q22 | KCNE1 | minK | Iks | < 1% | AD/AR | ||||
| LQTS6 | 21q22 | KCNE2 | MiRP1 | Ikr | < 1% | AD | ||||
| LQTS7 | 17q23 | KCNJ2 | Kir 2.1 | Ik1 | < 1% | AD | Anderson-Tawil-syndroom | |||
| LQTS8 | 6q8A | CACNA1C | (ICa-L) | < 1% | alternerende T-golven | Timothy-syndroom | ||||
| LQTS9 | 3p25.3 | CAV3 | Caveolin 3 | < 1% | ||||||
| LQTS10 | 11q23.3 | SCN4B | Navb4 | < 1% | ||||||
| LQTS11 | 7q21-q22 | AKAP9 | Caveolin 3 | 1 familie [3] | ||||||
| LQTS12 | 20q11.2 | Syntrophin-α1 | SNTA1 | 1 familie [4] |
Nog voordat deze genen bekend waren, waren er al enkele syndromen beschreven, die gepaard gingen met een lange QT-tijd.
- Anton Jervell and Fred Lange-Nielsen uit Oslo beschreven in 1957 een autosomaal recessief overervend syndroom dat gepaard ging met QT-verlenging, doofheid en plotselinge hartdood. Sindsdien heet dit syndroom Jervell-Lange-Nielsen-syndroom. [5]
- Romano-Ward-syndroom is een lange-QT-syndroom met normale gehoorfunctie en erft, i.t.t. de andere, autosomaal dominant over.
Inmiddels is bekend dat ook deze syndromen berusten op afwijkingen in bovenstaande genen.
Verworven LQTS
Verworven lange-QT-syndroom wordt meestal veroorzaakt door medicijnen. In combinatie met een aantal risicofactoren neemt het risico op ritmestoornissen toe, met name ook weer Torsade de Pointes.

| Medicijnen die Torsade de Pointes kunnen veroorzaken:[6] |
|---|
|
| Minder vaak gebruikte medicijnen: |
|
| Zie ook Torsades.org voor een uitgebreide lijst |
| Risicofactoren voor medicijngeïnduceerde Torsade de Pointes: |
|---|
|
Externe links
- LongQT.org Powerpoint presentatie over lange QT syndroom
- Torsades.org met een lijst met QT verlengende medicatie
- QTdrugs.org, met een lijst van QT verlengende medicatie
- Cardiogenetica.nl
- Sudden Arrhythmia Death Syndrome Foundation. Een Amerikaanse vereniging o.a. voor LQTS-patiënten.
- Inherited Arrhythmias Database
Referenties
- Goldenberg I, Mathew J, Moss AJ, McNitt S, Peterson DR, Zareba W, Benhorin J, Zhang L, Vincent GM, Andrews ML, Robinson JL, and Morray B. Corrected QT variability in serial electrocardiograms in long QT syndrome: the importance of the maximum corrected QT for risk stratification. J Am Coll Cardiol. 2006 Sep 5;48(5):1047-52. DOI:10.1016/j.jacc.2006.06.033 |
- Zipes DP, Camm AJ, Borggrefe M, Buxton AE, Chaitman B, Fromer M, Gregoratos G, Klein G, Moss AJ, Myerburg RJ, Priori SG, Quinones MA, Roden DM, Silka MJ, Tracy C, Smith SC Jr, Jacobs AK, Adams CD, Antman EM, Anderson JL, Hunt SA, Halperin JL, Nishimura R, Ornato JP, Page RL, Riegel B, Blanc JJ, Budaj A, Dean V, Deckers JW, Despres C, Dickstein K, Lekakis J, McGregor K, Metra M, Morais J, Osterspey A, Tamargo JL, Zamorano JL, American College of Cardiology/American Heart Association Task Force, European Society of Cardiology Committee for Practice Guidelines, European Heart Rhythm Association, and Heart Rhythm Society. ACC/AHA/ESC 2006 Guidelines for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death: a report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (writing committee to develop Guidelines for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death): developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. Circulation. 2006 Sep 5;114(10):e385-484. DOI:10.1161/CIRCULATIONAHA.106.178233 |
- Chen L, Marquardt ML, Tester DJ, Sampson KJ, Ackerman MJ, and Kass RS. Mutation of an A-kinase-anchoring protein causes long-QT syndrome. Proc Natl Acad Sci U S A. 2007 Dec 26;104(52):20990-5. DOI:10.1073/pnas.0710527105 |
- Ueda K, Valdivia C, Medeiros-Domingo A, Tester DJ, Vatta M, Farrugia G, Ackerman MJ, and Makielski JC. Syntrophin mutation associated with long QT syndrome through activation of the nNOS-SCN5A macromolecular complex. Proc Natl Acad Sci U S A. 2008 Jul 8;105(27):9355-60. DOI:10.1073/pnas.0801294105 |
- JERVELL A and LANGE-NIELSEN F. Congenital deaf-mutism, functional heart disease with prolongation of the Q-T interval and sudden death. Am Heart J. 1957 Jul;54(1):59-68. DOI:10.1016/0002-8703(57)90079-0 |
- Roden DM. Drug-induced prolongation of the QT interval. N Engl J Med. 2004 Mar 4;350(10):1013-22. DOI:10.1056/NEJMra032426 |
- Schwartz PJ, Priori SG, Spazzolini C, Moss AJ, Vincent GM, Napolitano C, Denjoy I, Guicheney P, Breithardt G, Keating MT, Towbin JA, Beggs AH, Brink P, Wilde AA, Toivonen L, Zareba W, Robinson JL, Timothy KW, Corfield V, Wattanasirichaigoon D, Corbett C, Haverkamp W, Schulze-Bahr E, Lehmann MH, Schwartz K, Coumel P, and Bloise R. Genotype-phenotype correlation in the long-QT syndrome: gene-specific triggers for life-threatening arrhythmias. Circulation. 2001 Jan 2;103(1):89-95. DOI:10.1161/01.cir.103.1.89 |
- Shah M, Akar FG, and Tomaselli GF. Molecular basis of arrhythmias. Circulation. 2005 Oct 18;112(16):2517-29. DOI:10.1161/CIRCULATIONAHA.104.494476 |
- Roden DM. Clinical practice. Long-QT syndrome. N Engl J Med. 2008 Jan 10;358(2):169-76. DOI:10.1056/NEJMcp0706513 |